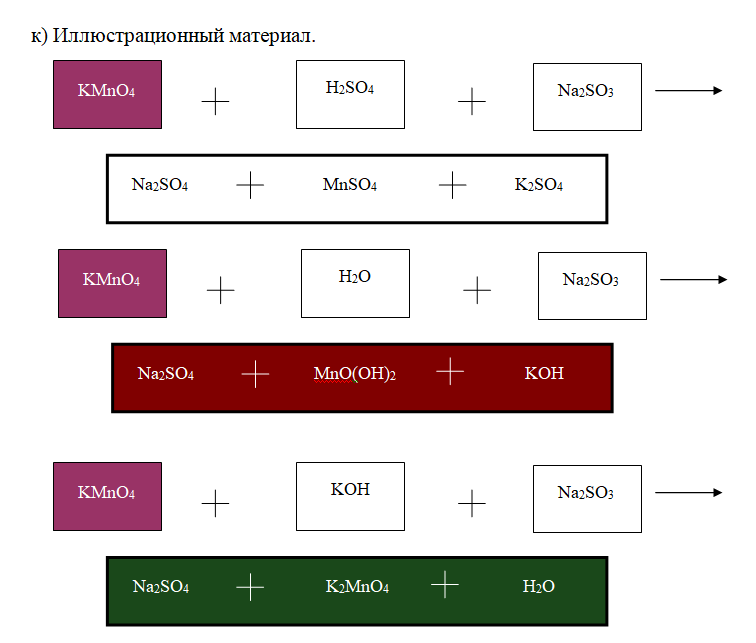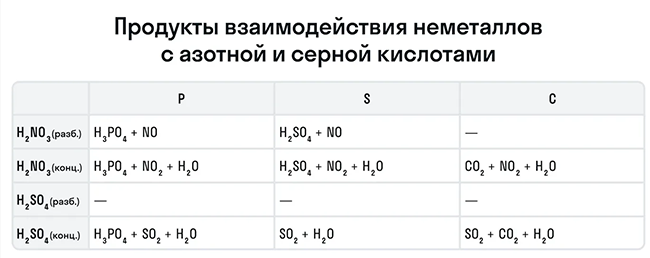
1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее.
Уточнить адрес. Стать продавцом. Покупать как компания. Мобильное приложение. Подарочные сертификаты.

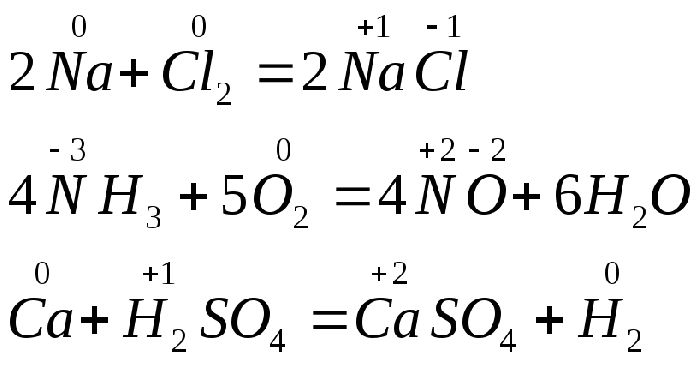

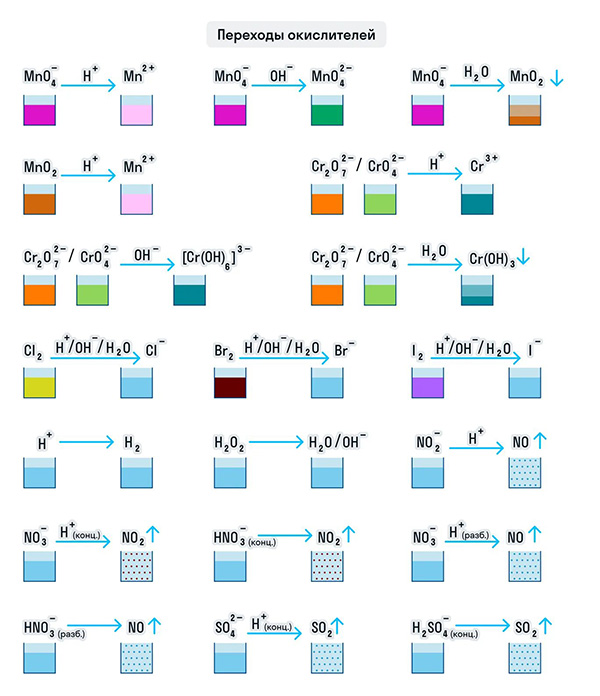

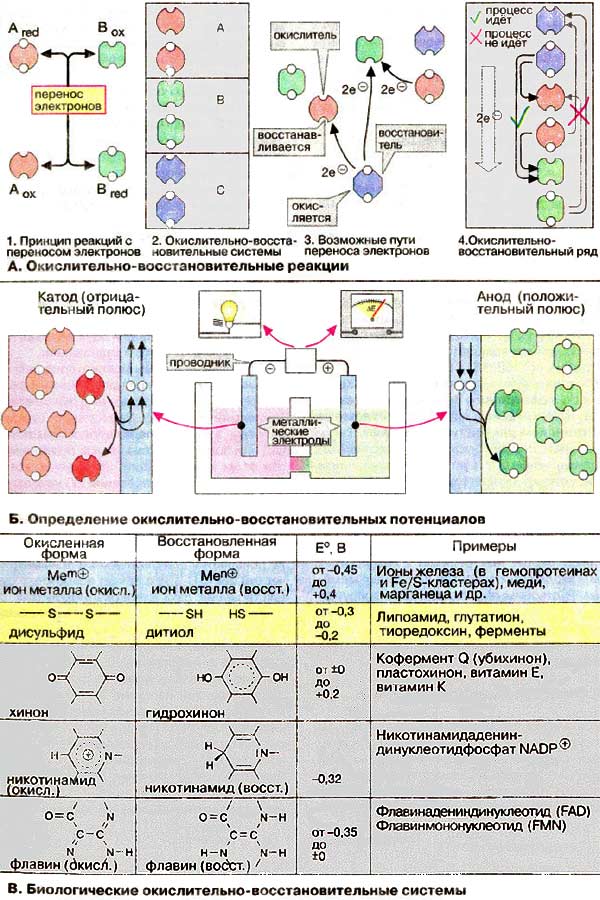


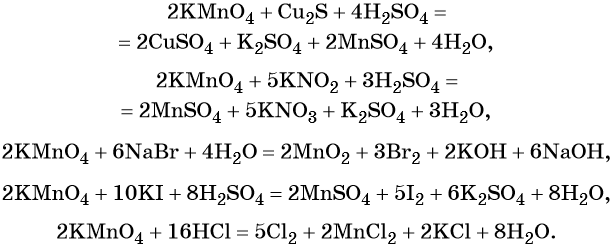
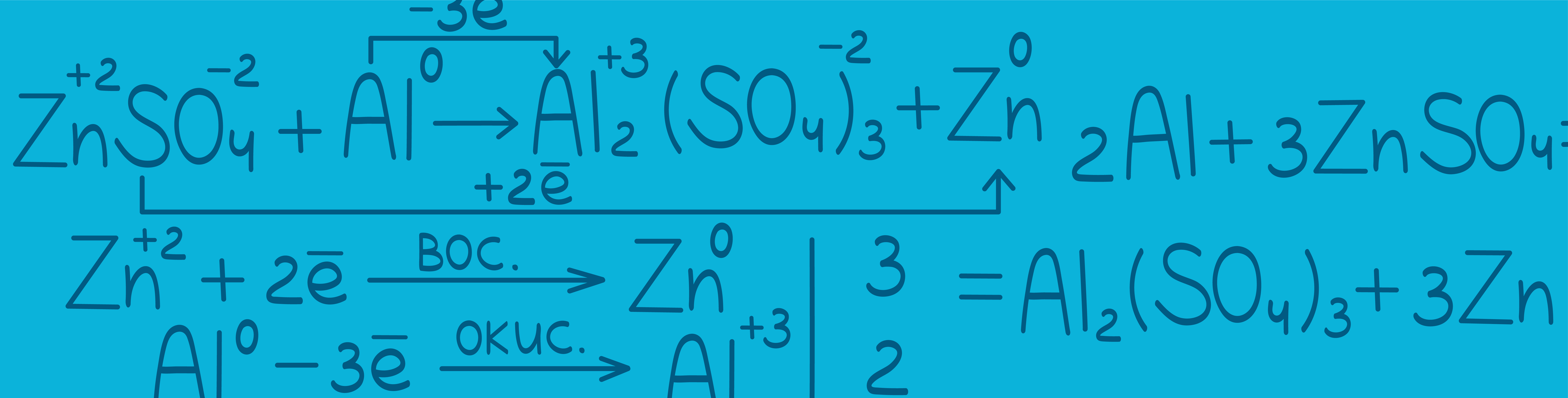
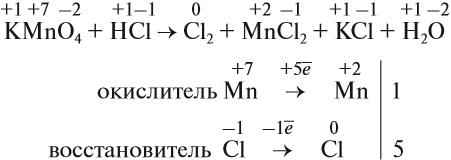
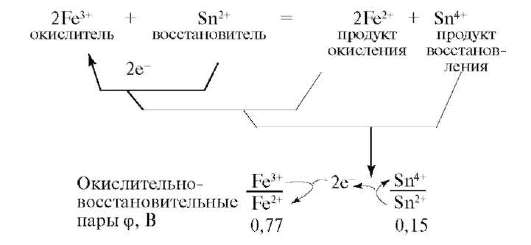
Окислительно-восстановительные реакции — это реакции, в которых происходит изменение степени окисления конкретных элементов, входящих в состав реагирующих друг с другом химических веществ. Это объясняется тем, что атомы способны обмениваться электронами друг с другом. Процесс окисления всегда происходит одновременно с восстановлением. Реакции отдачи и захвата электронов атомами записываются в виде полууравнений.
- Для расстановки коэффициентов в ОВР используют различные методы, среди которых наиболее часто применяют метод электронного баланса и метод полуреакций. В основе методов расстановки коэффициентов в ОВР лежит правило:.
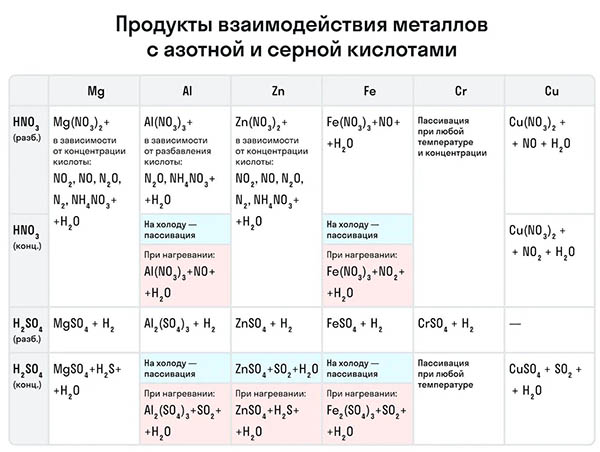
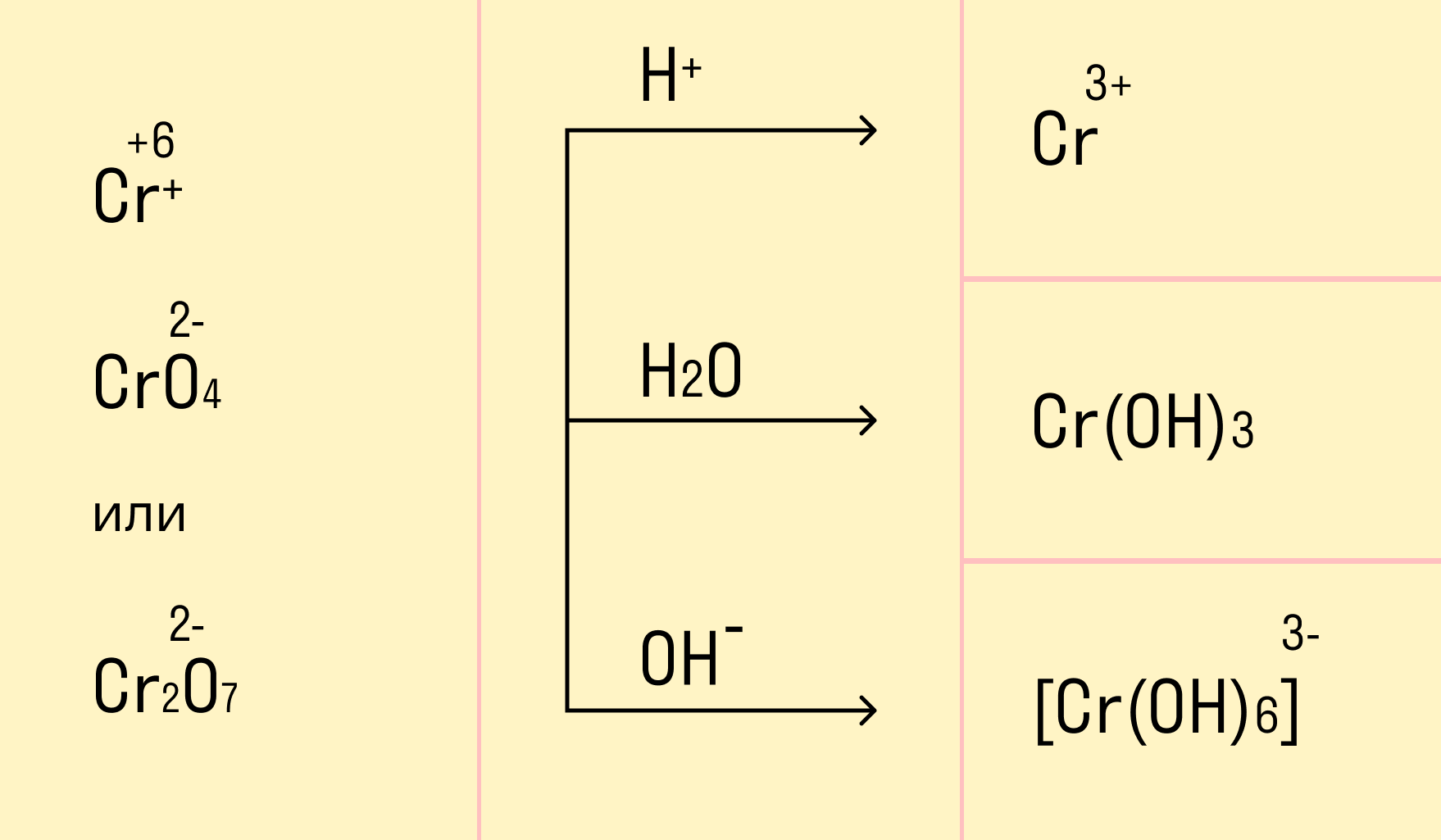
- Особенностью ОВР в растворах в частности, в водных является возможность участия в этих реакциях растворителя воды , а также продуктов автопротолиза растворителя в случае воды — ионов оксония и гидроксид-ионов. В случае водных растворов это приводит к возможности протекания между одними и теми же исходными веществами разных реакций в разных средах: кислотной, нейтральной или щелочной.
- Калькулятор ОВР - это способ составить уравнение электронного и массового баланса в уравнении окислительно-восстановительной реакции.
- Окислительно-восстановительные реакции ОВР — это реакции, при протекании которых происходит изменение степени окисления химических элементов, входящих в состав реагентов. Степень окисления — условный формальный заряд атома в химическом соединении, который находят, считая химические связи в соединении чисто ионными.
- Тема в программе: « Окислительно-восстановительные реакции » 8 класс. Тема урока: «Составление уравнений окислительно-восстановительных реакций методом электронного баланса».
- В ОВР органических веществ с неорганическими органические вещества чаще всего являются восстановителями.
- В молекулах пероксида водорода H 2 O 2 атомы кислорода находятся в степени окисления —I. Это промежуточная и не самая устойчивая степень окисления атомов этого элемента, поэтому пероксид водорода проявляет и окислительные, и восстановительные свойства.
- Степень окисления элементов. Во многих химических реакциях происходит перемещение электронов от одних частиц к другим.
- Окислительно-восстановительные реакции ОВР — такие реакции, которые протекают с изменением степеней окисления элементов.






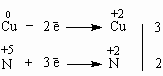

Для определения принадлежности той или иной реакции к окислительно-восстановительной, необходимо сделать следующее:. Если нет, то данная реакция не проявляет окислительно-восстановительных свойств. Нетрудно догадаться, что вещества, которые изменили степень окисления, могут быть либо окислителями, либо восстановителями.